共价键是一种化学键,它是由两个原子之间共用一对电子形成的。这种键在原子之间形成时,共用的电子对会使得两个原子都达到稳定的状态。
借助虚拟仿真可以将抽象的化学键以三维可视化的形式展示出来,使学生能够直观地看到电子的分布和原子之间的相互作用。
01
电负性
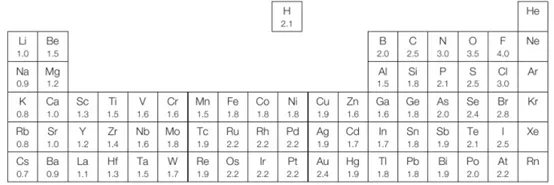
电负性是指原子吸引成键电子对的能力。
元素的电负性通常在元素周期表的一组中递减,也就是说,在一个周期内从左到右从上到下递增。
02
共价键的极性
如果同一元素的两个原子通过原子轨道的重叠结合在一起,则共用的电子对不会发生偏移。

Cl2分子的共用电子对不偏移
这是因为每个原子吸引成键电子对的能力是相同的。
然而,如果结合在一起的两个原子来自具有不同电负性的元素,那么电子对会发生偏移。

HCl分子的共用电子对向Cl原子偏移
可以看到共用电子对更靠近氯原子,这是因为氯原子具有更高的电负性。
由于共用电子对更靠近氯原子,所以分子的这一端带有轻微的负电荷,用符号δ-表示。分子的另一端带有轻微的正电荷,用符号δ+表示。

或者可以记作
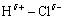
像这样子的键会称为极性共价键,或者简称为极性键。
END
















